某研究性学习小组在用CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,因为加热温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。为探究X的成分,他们进行了如下实验(图中①②表示试剂的加入顺序)。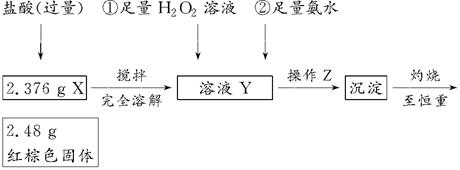
(1)操作Z是________。下列仪器中,在灼烧沉淀时必须用到的仪器名称是________;
(2)写出向溶液Y中滴加H2O2溶液时发生反应的离子方程式:________;
(3)通过以上数据,得出2.376 g黑色粉末X中各成分的物质的量为________。
某研究性学习小组在用CO还原Fe2O3的实验中,用磁铁吸出生成的黑色粉末X,他们认为X不一定是Fe,因为加热温度不同、受热不均时会生成Fe3O4,也能被磁铁吸引。为探究X的成分,他们进行了如下实验(图中①②表示试剂的加入顺序)。
(1)操作Z是________。下列仪器中,在灼烧沉淀时必须用到的仪器名称是________;
(2)写出向溶液Y中滴加H2O2溶液时发生反应的离子方程式:________;
(3)通过以上数据,得出2.376 g黑色粉末X中各成分的物质的量为________。