甲、乙两同学用下图所示装置进行实验,探究硝酸与铁反应的产物。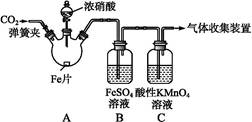
文献记载:Ⅰ.在浓硝酸与活泼金属反应过程中,随着硝酸浓度的降低,其生成的产物有+4、+2、-3价等氮的化合物。
Ⅱ.FeSO4+NO Fe(NO)SO4(棕色) ΔH<0。
Fe(NO)SO4(棕色) ΔH<0。
Ⅲ.NO2和NO都能被KMnO4氧化吸收。
甲的实验操作和现象记录如下:
| 实验操作 |
实验现象 |
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹。 |
|
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞。 |
无明显现象。 |
| 加热烧瓶,反应开始后停止加热。 |
①A中有红棕色气体产生,一段时间后,气体颜色逐渐变浅;B中溶液变棕色;C中溶液紫色变浅。 ②反应停止后,A中无固体剩余。 |
请回答下列问题:
(1)滴入浓硝酸加热前没有明显现象的原因是 。
(2)检验是否生成-3价氮的化合物,应进行的实验操作是 。
(3)甲取少量B中溶液,加热,实验现象是 。请用化学平衡原理解释原因: 。甲依据该现象得出的结论是A中有NO生成。
(4)乙认为甲得出A中有NO生成的证据不足。为获取充足的证据,乙仍采用该装置和操作进行对照实验,乙作出的改变是 ,证明有NO生成的实验现象是 。
(5)证明A溶液中含有Fe3+,选择的药品是(填序号) 。
A.铁粉 B.溴水 C.铁氰化钾溶液 D.硫氰化钾溶液
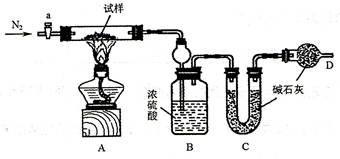
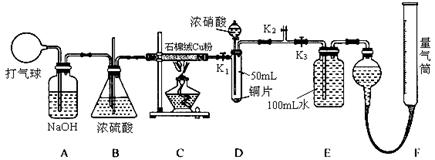

 N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。


 粤公网安备 44130202000953号
粤公网安备 44130202000953号