通过实验制取并验证二氧化碳的某些性质。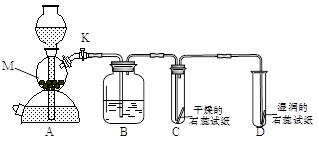
(1)开始实验前装置如图所示,M处应盛放_ 。打开活塞K,观察到的现象是_ ,发生反应的化学方程式是_ 。
(2)为了使实验结论科学、可靠,B装置的作用是_ ,该实验可知二氧化碳的化学性质是 。
(3)实验结束后,关闭活塞K,固液未分离,可能的原因是 。
通过实验制取并验证二氧化碳的某些性质。
(1)开始实验前装置如图所示,M处应盛放_ 。打开活塞K,观察到的现象是_ ,发生反应的化学方程式是_ 。
(2)为了使实验结论科学、可靠,B装置的作用是_ ,该实验可知二氧化碳的化学性质是 。
(3)实验结束后,关闭活塞K,固液未分离,可能的原因是 。