利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤。
已知:SO2(g)+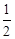 O2(g)
O2(g) SO3(g) △H=-98 kJ·mol-1。
SO3(g) △H=-98 kJ·mol-1。
(1)某温度下该反应的平衡常数K=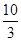 ,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”)。
,若在此温度下,向100 L的恒容密闭容器中,充入3.0 mol SO2(g)、16.0 mol O2(g)和3.0 mol SO3(g),则反应开始时v(正) v(逆)(填“<”、“>”或“=”)。
(2)一定温度下,向一带活塞的体积为2 L的密闭容器中充入2.0 mol SO2和1.0 molO2,达到平衡后体积变为1.6 L,则SO2的平衡转化率为 。
(3)在(2)中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是 (填字母)。
| A.保持温度和容器体积不变,充入1.0 mol O2 |
| B.保持温度和容器内压强不变,充入1.0 mol SO3 |
| C.降低温度 |
| D.移动活塞压缩气体 |
(4)若以如图所示装置,用电化学原理生产硫酸, 写出通入O2电极的电极反应式为 。
(5)为稳定持续生产,硫酸溶液的浓度应维持不变,则通入SO2和水的质量比为_____。



 既能起银镜反应,遇FeCl3溶液又能呈紫色的同分异构体的结构简式 。
既能起银镜反应,遇FeCl3溶液又能呈紫色的同分异构体的结构简式 。 )为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
)为基本原料,经过反应得到一系列的芳炔类大环化合物,其结构为:
 无机试剂自选)
无机试剂自选) 2C(g)+2D(g),2 min末反应达到
2C(g)+2D(g),2 min末反应达到 平衡状态,生成了0.8 mol D,请填写下列空白:
平衡状态,生成了0.8 mol D,请填写下列空白: 然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内
然界的矿物、岩石的成因和变化受到许多条件的影响。地壳内每加深1km,压强增大约25000~30000 kPa。在地壳内 SiO2和HF存在以下平衡:SiO2 (s) + 4HF(g)
SiO2和HF存在以下平衡:SiO2 (s) + 4HF(g)  SiF
SiF 4 (g) + 2H2O(g)
4 (g) + 2H2O(g)  述反应的平衡常数K值变大,该反应_________(选填编号)。
述反应的平衡常数K值变大,该反应_________(选填编号)。 反应速率先减小后增大
反应速率先减小后增大 粤公网安备 44130202000953号
粤公网安备 44130202000953号