常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中不正确的是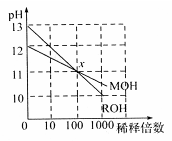
| A.ROH是一种强碱 |
| B.等物质的量浓度的MOH与盐酸反应,所得溶液呈中性,则MOH的体积大于盐酸的体积 |
| C.在x点,c(M+)=c(R+) |
| D.稀释前,c(ROH)=10 c(MOH) |
常温下MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如图所示。下列叙述中不正确的是
| A.ROH是一种强碱 |
| B.等物质的量浓度的MOH与盐酸反应,所得溶液呈中性,则MOH的体积大于盐酸的体积 |
| C.在x点,c(M+)=c(R+) |
| D.稀释前,c(ROH)=10 c(MOH) |