铝是一种应用广泛的金属,工业上用和冰晶石()混合熔融电解制得。
①铝土矿的主要成分是和等。从铝土矿中提炼的流程如下:

②以萤石()和纯碱为原料制备冰晶石的流程如下:
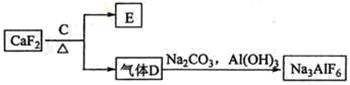
回答下列问题:
(1)写出反应1的化学方程式
(2)滤液Ⅰ中加入生成的沉淀是
(3)可作为建筑材料,化合物是
(4)电解制铝的化学方程式是
铝是一种应用广泛的金属,工业上用和冰晶石()混合熔融电解制得。
①铝土矿的主要成分是和等。从铝土矿中提炼的流程如下:

②以萤石()和纯碱为原料制备冰晶石的流程如下:

回答下列问题:
(1)写出反应1的化学方程式
(2)滤液Ⅰ中加入生成的沉淀是
(3)可作为建筑材料,化合物是
(4)电解制铝的化学方程式是