下列实验可达到实验目的的是:
①将 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
②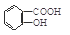 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备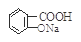
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴水即可检验CH2=CH-CHO中的碳碳双键
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |
下列实验可达到实验目的的是:
①将 与NaOH的醇溶液共热制备CH3—CH═CH2
与NaOH的醇溶液共热制备CH3—CH═CH2
②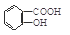 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备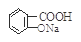
③向CH3CH2Br中滴入AgNO3溶液以检验溴元素
④用溴水即可检验CH2=CH-CHO中的碳碳双键
| A.只有① | B.只有①④ | C.只有①③④ | D.都不能 |