海水的综合利用可以制备金属钠和镁,其流程如下图所示: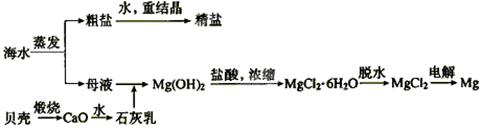
(1)上述流程中生成氢氧化镁沉淀的离子方程式为 。氢氧化镁沉淀和盐酸反应的离子方程式为 。
(2)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:____________;过滤时:____________;蒸发时:______________。
海水的综合利用可以制备金属钠和镁,其流程如下图所示:
(1)上述流程中生成氢氧化镁沉淀的离子方程式为 。氢氧化镁沉淀和盐酸反应的离子方程式为 。
(2)实验室里将粗盐制成精盐的过程中,在溶解、过滤、蒸发三个步骤的操作中都要用到玻璃棒,分别说明这三种情况下使用玻璃棒的作用:
溶解时:____________;过滤时:____________;蒸发时:______________。