孔雀石主要含Cu2(OH)2CO3,还含少量Fe的氧化物和SiO2,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:

试回答下列问题:
(1)B物质的化学式是在未加入H2O2的溶液中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是(填代号)。
| A.KMnO4溶液 |
B.Fe粉 |
C.Na2CO3溶液 |
D.KSCN溶液 |
(2)向溶液A加入H2O2的作用是剂(填氧化或还原),离子反应方程式为,选用H2O2而不用Cl2的原因是。
(3)由溶液C获得CuSO4·5H2O,需要经过,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器是。
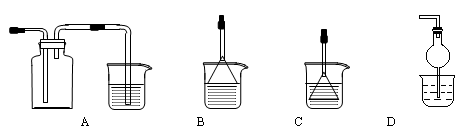
(4)制备CaCO3时,先通入(填NH3或CO2),若实验过程中有氨气逸出,可选用下列装置中的 (填代号)装置吸收氨气。(烧杯中的液体都为水)