酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60;
②核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:乙醇(CH3CH2OH)有三种氢原子(图1).经测定,有机物A的核磁共振氢谱示意图如图2: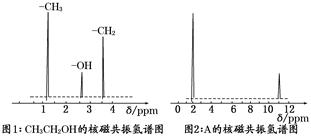
③对A的水溶液进行测定发现该溶液pH<7.
根据以上分析,写出A的结构简式________.
酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下分析:
①通过样品的质谱分析测得A的相对分子质量为60;
②核磁共振氢原子光谱能对有机物分子中同性氢原子给出相同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:乙醇(CH3CH2OH)有三种氢原子(图1).经测定,有机物A的核磁共振氢谱示意图如图2:
③对A的水溶液进行测定发现该溶液pH<7.
根据以上分析,写出A的结构简式________.