如下图所示,将三支充满二氧化碳的试管分别倒立在盛有水、澄清石灰水、浓氢氧化钠溶液中进行实验,请按要求回答相关问题: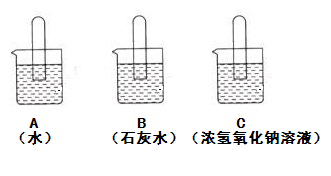
(提示:图示中呈现的是实验过程中的试管内液面的高度,不是最终的现象)
(1)B中的实验现象是 ,反应的化学方程式为 。
(2)证明A中二氧化碳能与水反应的方法是 。
(3)是否可以通过上述实验中的最终现象,证明二氧化碳能与氢氧化钠反应,其理由是 。
如下图所示,将三支充满二氧化碳的试管分别倒立在盛有水、澄清石灰水、浓氢氧化钠溶液中进行实验,请按要求回答相关问题:
(提示:图示中呈现的是实验过程中的试管内液面的高度,不是最终的现象)
(1)B中的实验现象是 ,反应的化学方程式为 。
(2)证明A中二氧化碳能与水反应的方法是 。
(3)是否可以通过上述实验中的最终现象,证明二氧化碳能与氢氧化钠反应,其理由是 。