叠氮化钠(NaN3)被广泛应用于汽车安全气囊,某化学小组同学对其进行下列研究。
【查阅资料】
①NaN3受撞击会生成Na、N2。
②NaN3遇盐酸、H2SO4溶液无气体生成。
③碱石灰是CaO和 NaOH的混合物。
④NaN3的制备方法是:将金属钠与液态氨反应制得NaNH2,再将NaNH2与N2O反应可生成NaN3、NaOH和氨气(NH3)。
【问题探究】
(1)汽车经撞击后,30毫秒内引发NaN3迅速分解,写出该反应的化学方程式 。
(2)工业级NaN3中常含有少量的Na2CO3,其原因是(用化学方程式表示) 。
(3)为测定某工业级NaN3样品中含有Na2CO3的质量分数,化学小组同学设计了如下实验装置。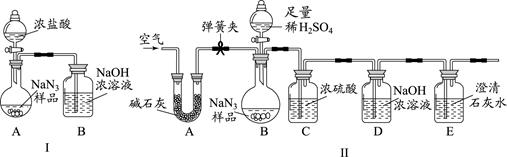
①小明同学认为通过测定装置Ⅰ中反应前后B的质量差,再通过相应计算,就可测定Na2CO3的纯度,小组内同学通过讨论认为不可以,其理由可能是 。ⅠⅡ
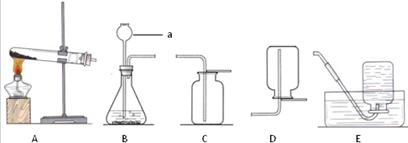
②小刚同学在大家讨论的基础上,设计了装置Ⅱ。请分析:装置Ⅱ中A的作用是_____;若无装置C,对测定结果造成的影响是 (填“偏大”、“偏小”或“无影响”);装置E的作用是 。
③根据装置Ⅱ,小组同学设计的实验步骤有:a.称量装置D。b.称量样品,检查装置气密性。c.打开弹簧夹,鼓入空气。d.打开分液漏斗的活塞和玻璃塞,注入足量的稀硫酸,关闭活塞和玻璃塞。其正确顺序为 (填字母序号,可重复)。

 粤公网安备 44130202000953号
粤公网安备 44130202000953号