将体积为100 mL浓度为2.0 mol·L־1 的CuSO4溶液和体积为300 mL浓度为1.0 mol·L־1 的H2SO4溶液混合,假定混合后溶液体积为400 mL。计算:
(1)混合液中CuSO4的物质的量浓度是 ,H2SO4的物质的量浓度是 。
(2)往混合液中加水稀释至Cu2+ 浓度为0.2 mol·L־1,则稀释后溶液的体积为 。
(3)稀释后溶液中H+ 的物质的量浓度是 ,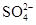 的物质的量浓度是 。
的物质的量浓度是 。
将体积为100 mL浓度为2.0 mol·L־1 的CuSO4溶液和体积为300 mL浓度为1.0 mol·L־1 的H2SO4溶液混合,假定混合后溶液体积为400 mL。计算:
(1)混合液中CuSO4的物质的量浓度是 ,H2SO4的物质的量浓度是 。
(2)往混合液中加水稀释至Cu2+ 浓度为0.2 mol·L־1,则稀释后溶液的体积为 。
(3)稀释后溶液中H+ 的物质的量浓度是 ,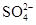 的物质的量浓度是 。
的物质的量浓度是 。