肉桂醛(C9H8O)是一种常用香精,在食品、医药化工等方面都有应用。肉桂醛与其他有机物具有如下转化关系,其中A为一氯代烃。
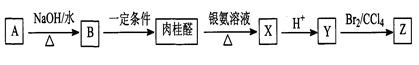
(1)肉桂醛是苯的一取代物,与H2加成的产物中没有支链,肉桂醛结构简式是。
(2)反应A→B的化学方程式是________________________________。
(3)Z不能发生的反应类型是(填字母)___________。
a. 取代反应 b. 加聚反应 c. 加成反应 d. 消去反应
(4)Y与乙醇在一定条件下反应的化学方程式是:____________________。
(5)写出符合下列条件的Y的一种同分异构体的结构:______________________________。
①属于酯类②苯环上只有一个取代基③能发生银镜反应。