某学生采用下面的装置及实验方法来测定推断乙醇的分子结构。
(1)该学生分别准备称取4.60 g乙醇进行多次实验,结果发现已排到量筒内的水的体积作为生成氢气的体积换算成标准状况下的体积都小于1.12 L。若忽略量筒本身及读数造成的误差,那么该学生认为是由于样品中含有少量水造成的,你认为正确吗?_________________(填“正确”或“不正确”)。如果你认为正确,请说明理由;你认为不正确,那么产生这种情况的原因应是什么?
____________________________________________________________。
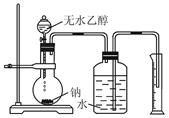
(2)该学生认为实验成功的关键有:
①装置气密性良好 ②实验开始前要准确确定乙醇的量 ③钠足量 ④广口瓶内必须充满水 ⑤氢气的体积测算方法正确、数据准确
你认为,其中正确的有_______________(填序号)。
(3)实验后,该学生从乙醇的可能结构分析入手,对乙醇和钠的关系进行讨论,若乙醇的物质的量为n mol,则对钠的物质的量取值要求必须是________________。