如图装置可验证二氧化碳和氢氧化钠发生了化学反应:将等量的氢氧化钠溶液和蒸馏水分别加入两瓶等量二氧化碳气体中,用
型管连接.充分反应后放在水平桌面上可观察到
型管中液面出现高度差.
(1)室温下利用此装置,你还可以研究.
A.比较氧气和二氧化碳在水中的溶解能力
B.比较氯酸钾和氯化钠在水中的溶解能力
C.比较饱和氢氧化钠和氢氧化钙溶液吸收二氧化碳气体的能力
(2)进一步思考、迁移:有变化的对比实验都可以用此装置进行探究.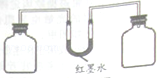
如图装置可验证二氧化碳和氢氧化钠发生了化学反应:将等量的氢氧化钠溶液和蒸馏水分别加入两瓶等量二氧化碳气体中,用
型管连接.充分反应后放在水平桌面上可观察到
型管中液面出现高度差.
(1)室温下利用此装置,你还可以研究.
A.比较氧气和二氧化碳在水中的溶解能力
B.比较氯酸钾和氯化钠在水中的溶解能力
C.比较饱和氢氧化钠和氢氧化钙溶液吸收二氧化碳气体的能力
(2)进一步思考、迁移:有变化的对比实验都可以用此装置进行探究.