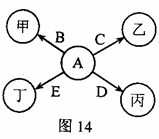
图14所示的是几种常见物质的转化关系,其中
是单质,甲、乙、丙、丁是氧化物.已知:丙是红色固体,
是最清洁的燃料,丙高温下与乙反应可生成
.(部分反应物、生成物及反应条件己略去)
请回答下列问题:
(1)丁的化学式为;
(2)甲的化学式可能为(只写一种);
(3)丙与乙反应的化学方程式为:;
(4)写出
的一条用途:.
图14所示的是几种常见物质的转化关系,其中
是单质,甲、乙、丙、丁是氧化物.已知:丙是红色固体,
是最清洁的燃料,丙高温下与乙反应可生成
.(部分反应物、生成物及反应条件己略去)
请回答下列问题:

(1)丁的化学式为;
(2)甲的化学式可能为(只写一种);
(3)丙与乙反应的化学方程式为:;
(4)写出
的一条用途:.