根据下图回答以下问题: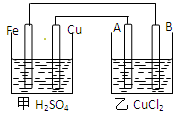
(A、B均为碳棒,两池中溶液均足量)
(1)甲装置是 池,乙装置是 池且Fe极为 极,A极为 极
(2)A极的电极反应
(3)若甲池中Fe溶解0.3 mol,则乙池中产生气体的总体积(标准状况)为 L,
乙池 极质量会增加 g
根据下图回答以下问题:
(A、B均为碳棒,两池中溶液均足量)
(1)甲装置是 池,乙装置是 池且Fe极为 极,A极为 极
(2)A极的电极反应
(3)若甲池中Fe溶解0.3 mol,则乙池中产生气体的总体积(标准状况)为 L,
乙池 极质量会增加 g