某有机物X(C12H14O7)的分子中含有多种官能团,其结构简式为:

(其中R1、R2为未知部分的结构),已知X可以发生如图所示的转化:
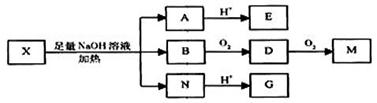
已知1)向X、E的水溶液中滴入FeCl3溶液均发生显色反应; 2)E的核磁共振谱图中只有两个峰,面积比为1:2; 3)G、M(C2H2O4)都能与NaHCO3溶液反应。
(1)写出X的结构简式为。
(2)1molX与NaOH溶液反应时,消耗mol NaOH。
(3)E的结构简式是;B的命名为_____________________
①写出B转化成D的化学方程式:___________ __________
②写出A溶液与CO2反应的离子方程式:________________ _________。
H与G互为同分异构体,H的分子中只含有醛基、羧基、羟基三种官能团,且同一个碳原子上不 能同时连有两个羟基,则H的分子结构有______种.