下图转化关系中,化合物B既能使溴的CCl4溶液褪色,又能与NaHCO3溶液反应生成无色气体;D、E均为高分子化合物;已知一个碳原子同时连接两个羟基的结构不稳定。根据下图填空: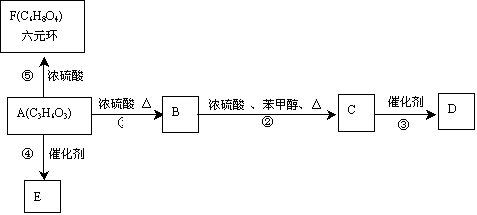
(1)A的结构简式是 ;B中含有官能团名称是 ;
(2)反应③的化学方程式是 ;
(3)反应①的反应类型是 ;
(4)高分子化合物E可作为可降解塑料,E的结构简式是 ;
下图转化关系中,化合物B既能使溴的CCl4溶液褪色,又能与NaHCO3溶液反应生成无色气体;D、E均为高分子化合物;已知一个碳原子同时连接两个羟基的结构不稳定。根据下图填空:
(1)A的结构简式是 ;B中含有官能团名称是 ;
(2)反应③的化学方程式是 ;
(3)反应①的反应类型是 ;
(4)高分子化合物E可作为可降解塑料,E的结构简式是 ;