A、B、C、D、E、F均为前四周期的元素,原子序数依次增大,A的核外电子数等于其电子层数,B的最外层电子数是次外层电子数的3倍,A和C、B和E同主族,B、C、D的离子具有相同的电子层结构,D的离子是同周期中离子半径最小的,F原子中共有6个未成对电子。
请回答下列问题:
⑴写出下列元素的元素符号:A ▲ 、C ▲ 、E ▲ 、F ▲ 。
⑵元素A和元素B可以形成A2B物质甲,写出甲的分子式 ▲ ,甲为 ▲ (填“极性”或“非极性”)分子。
⑶元素A和元素E形成化合物乙,用电子式表示化合物乙 ▲ ;常温下甲为液态,乙为气态,试解释原因 ▲ 。
⑷元素A与元素C形成化合物丙,丙的水溶液显碱性,试用化学方程式解释其原因:
▲ 。
⑸元素C、元素D的最高价氧化物的水化物相互反应的离子方程式是 ▲ 。
⑹写出元素F的外围电子排布式 ▲ 。

 CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下:
CO(NH2)2 (l) + H2O (l),该反应的平衡常数和温度关系如下: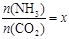 ,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是_______。
,下图是氨碳比(x)与CO2平衡转化率(α)的关系。α随着x增大而增大的原因是_______。


 CH3OH(g)。若不考虑生产过 程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2mol。
CH3OH(g)。若不考虑生产过 程中物质的任何损失,上述产业链中每合成6mol甲醇,至少需额外补充H2mol。 粤公网安备 44130202000953号
粤公网安备 44130202000953号