氨气极易溶于水,常温常压下1体积水可溶解700体积的氨气,溶解后可与水反应生成一水合氨,溶液显碱性。氨气的密度比空气小。已知:
2NH4Cl(固体)+ Ca(OH)2(固体) 2NH3↑+ CaCl2 + 2H2O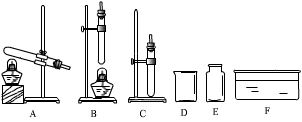
(l)如果制取并收集保存氨气,请从上图中选取装置和仪器 (填序号)。
(2)氨气不能用排水法收集,原因是 。
氨气极易溶于水,常温常压下1体积水可溶解700体积的氨气,溶解后可与水反应生成一水合氨,溶液显碱性。氨气的密度比空气小。已知:
2NH4Cl(固体)+ Ca(OH)2(固体) 2NH3↑+ CaCl2 + 2H2O
(l)如果制取并收集保存氨气,请从上图中选取装置和仪器 (填序号)。
(2)氨气不能用排水法收集,原因是 。