某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分
),要求全过程不引入其他金属元素。设计实验方案如下图所示,
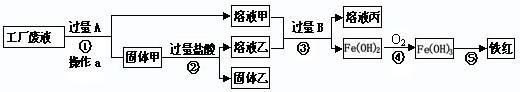 |
回答下列问题。
(1)加入过量
溶解后,再进行操作a时玻璃棒的作用是
(2)工厂废液中加入过量
反应的化学方程式为
(3)溶液甲中的金属离子是
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是
(5)铁红是炼铁的主要原料,写出用
和铁红炼铁的化学方程式
某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分
),要求全过程不引入其他金属元素。设计实验方案如下图所示,
 |
回答下列问题。
(1)加入过量
溶解后,再进行操作a时玻璃棒的作用是
(2)工厂废液中加入过量
反应的化学方程式为
(3)溶液甲中的金属离子是
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是
(5)铁红是炼铁的主要原料,写出用
和铁红炼铁的化学方程式