已知—NH2连在苯环上显碱性,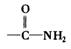 连在苯环上显中性,化学式为C7H7NO2
连在苯环上显中性,化学式为C7H7NO2
的有机物中其分子结构中有一个苯环,两个侧链(间位),符合下列条件的结构简式为:
(1)既有酸性又有碱性__________________(2)只有酸性_______________
(3)只有碱性___________________ (4)显中性___________________
已知—NH2连在苯环上显碱性,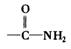 连在苯环上显中性,化学式为C7H7NO2
连在苯环上显中性,化学式为C7H7NO2
的有机物中其分子结构中有一个苯环,两个侧链(间位),符合下列条件的结构简式为:
(1)既有酸性又有碱性__________________(2)只有酸性_______________
(3)只有碱性___________________ (4)显中性___________________