把aL含硫酸铵和硝酸铵的混合液分成两等份,一份需用b molNaOH刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol BaCl2,由此可知原溶液中NO3—的物质的量浓度是(单位:mol·L—1)
A.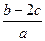 |
B.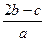 |
C.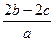 |
D.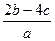 |
把aL含硫酸铵和硝酸铵的混合液分成两等份,一份需用b molNaOH刚好把氨全部赶出,另一份与氯化钡溶液反应时,消耗c mol BaCl2,由此可知原溶液中NO3—的物质的量浓度是(单位:mol·L—1)
A.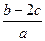 |
B.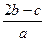 |
C.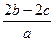 |
D.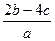 |