(12分)A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如下所示转化关系。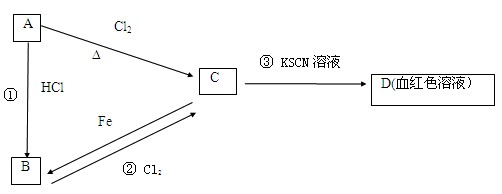
试回答下列问题:
(1)A是 ,C是 。
(2)C的溶液与NaOH溶液混合后的现象是 。
(3)反应①的反应类型是 反应(选填“化合”“分解”“置换”“复分解”)。
(12分)A、B、C、D四种物质都含有一种共同的元素,A是常见的金属,C的溶液呈现黄色,A、B、C、D之间有如下所示转化关系。
试回答下列问题:
(1)A是 ,C是 。
(2)C的溶液与NaOH溶液混合后的现象是 。
(3)反应①的反应类型是 反应(选填“化合”“分解”“置换”“复分解”)。