某化工厂以软锰矿、闪锌矿(除主要成分为MnO2、ZnS外还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2。
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,配平如下的化学方程式:
MnO2 + FeS + H2SO4 MnSO4 + Fe2(SO4)3 + S + H2O
MnSO4 + Fe2(SO4)3 + S + H2O
(2)将所得含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液按以下的工业流程进行操作处理得溶液(IV),电解溶液(IV)即得MnO2和Zn。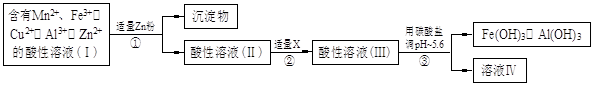
a.操作①中加Zn粉后发生反应的离子方程式为 。
b.操作②中加入适量X的作用是什么 ;X的首选物的化学式是 。
c.操作③中所加碳酸盐的化学式是 。
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如下的有关流程图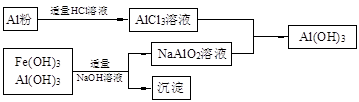
a.AlCl3溶液和NaAlO2溶液反应生成AI(OH)3的离子方程式为 ,若总共得到n molAl(OH)3,则消耗的NaOH和HCl的理论量(mol)分别为 、 。
b.若使用下列流程回收处理,请比较两个流程消耗酸碱的用量?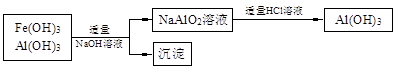
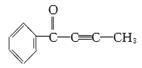 。根据M的结构回答:M中不饱和碳原子有
。根据M的结构回答:M中不饱和碳原子有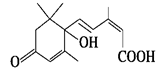 。根据S诱抗素结构,可知S诱抗素分子中含有的官能团有 、 、 、 。
。根据S诱抗素结构,可知S诱抗素分子中含有的官能团有 、 、 、 。
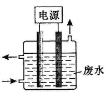
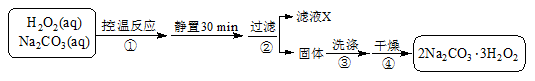
 2Na2CO3·3H2O2(s)ΔH<0,请回答下列问题:
2Na2CO3·3H2O2(s)ΔH<0,请回答下列问题: 粤公网安备 44130202000953号
粤公网安备 44130202000953号