在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如右图所示。则:
(1)原溶液中Mg2+、Al3+物质的量浓度之比为___________。
(2)图中C点表示当加入______molNaOH时,Al3+已经转变为_______,Mg2+已经转变为_________。
(3)图中线段OA∶AB=___________。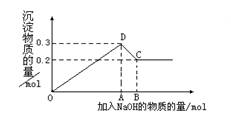
在MgCl2和AlCl3的混合溶液中,逐滴加入NaOH溶液直至过量。经测定,加入的NaOH的物质的量(mol)和所得沉淀的物质的量(mol)的关系如右图所示。则:
(1)原溶液中Mg2+、Al3+物质的量浓度之比为___________。
(2)图中C点表示当加入______molNaOH时,Al3+已经转变为_______,Mg2+已经转变为_________。
(3)图中线段OA∶AB=___________。