汽车尾气中的主要污染物是NO以及燃料不完全燃烧所产生的CO。为了减轻大气污染,人们提出通过以下反应来处理汽车尾气:2NO(g)+2CO(g)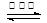 2CO2(g)+N2(g) ΔH =" a" kJ·mol-1
2CO2(g)+N2(g) ΔH =" a" kJ·mol-1
为了测定在某种催化剂作用下该反应的反应速率,t1℃下,在一定容的密闭容器中,某科研机构用气体传感器测得了不同时间的NO和CO的浓度如下表(CO2和N2的起始浓度均为0)。
时间 (s)
|
0
|
1
|
2
|
3
|
4
|
5
|
c(NO)/10-4mol/L
|
10.0
|
4.50
|
2.50
|
1.50
|
1.00
|
1.00
|
c(CO)/10-3mol/L
|
3.60
|
3.05
|
2.85
|
2.75
|
2.70
|
2.70
|
回答下列问题:
(1)在上述条件下该反应能自发进行,则正反应必然是_______反应(填“放热”或“吸热”)。
(2)前3s内的平均反应速率υ(N2)=______________,t1℃时该反应的平衡常数K=____________。
(3)t1℃时向一恒压容器中冲入1molNO和1molCO,达到平衡时测得NO的物质的量为0.2mol,则此时容器的体积V=" ________" L。
(4)假设在密闭容器中发生上述反应,达到平衡时改变下列条件,能提高NO转化率的是_____。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度D.缩小容器的体积