标准状况下,向100mLNaOH溶液中慢慢通入CO2气体充分反应后,在所得溶液M中逐滴加入1mol/L盐酸,(反应前后溶液体积变化忽略不计)所得气体体积和所加盐酸的体积关系如图。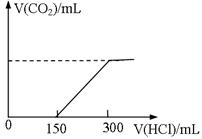
(1)c(NaOH)=
(2)取M溶液40mL与等体积的1mol/L盐酸按各种可能方式混合,产生气体的体积为VmL,则V的取值范围为 。
标准状况下,向100mLNaOH溶液中慢慢通入CO2气体充分反应后,在所得溶液M中逐滴加入1mol/L盐酸,(反应前后溶液体积变化忽略不计)所得气体体积和所加盐酸的体积关系如图。
(1)c(NaOH)=
(2)取M溶液40mL与等体积的1mol/L盐酸按各种可能方式混合,产生气体的体积为VmL,则V的取值范围为 。