用18 mol/L浓硫酸配制100ml 3.0mol/L稀硫酸实验步骤如下:①计算所用硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀
回答下列问题:
(1)所需浓硫酸的体积是_________ml;
(2)所需要的仪器有:容量瓶(规格:__________)、量筒(规格:__________)
(从下列中选用填序号:A、10ml B、25ml C、500ml D、250ml E、100ml),
除此之外还需要的仪器有:____________________________________________________。
(3)下列情况对所配制的稀硫酸浓度有何影响?(用偏高、偏低、无影响填写)
A、所用的溶解仪器未洗涤_________________;
B、容量瓶用蒸馏水洗涤后未干燥_________________;
C、所用的浓硫酸长时间放置在敞口容器内_________________;
D、定容时仰视溶液的凹液面_________________;
E、溶解后立即转移到容量瓶中定容_________________。
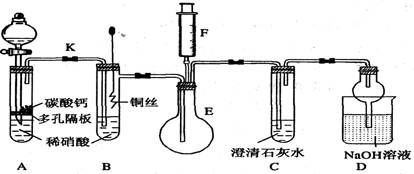
 。某课题组用
为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。
。某课题组用
为原料模拟该过程,探究上述反应的实验条件及固体产物的成分。



 粤公网安备 44130202000953号
粤公网安备 44130202000953号