实验室可利用乙二醇、铜或铜的化合物制备乙二醛,右图是某兴趣小组设计的实验装置,右边的反应装置相同,而左边的气体发生装置不同,试管C中装有水(加热装置未画出)。试回答:
(1)两套装置中的A、B处都需加热,
A处用水浴加热,B处用 ▲ 加热,A处用水浴加热的主要优点是 ▲ 。
(2)若按甲装置进行实验,B管处装铜粉,则通入A管的X是 ▲ ,
B中反应的化学方程式为 ▲ 。
(3)若按乙装置进行实验,则B管中应装 ▲ ,B中反应的化学方程式为 ▲ 。
(4)实验完成时先打开D处的铁夹,再撤去酒精灯,试说明这样做的目的是 ▲ 。
 O3② H2SO4③ CH3COOH④ Ba(OH)2⑤ NaOH⑥ CH3COONa⑦ KCl⑧ NH4Cl,溶液PH由大到小的顺序是(填写编号)_________________________________
O3② H2SO4③ CH3COOH④ Ba(OH)2⑤ NaOH⑥ CH3COONa⑦ KCl⑧ NH4Cl,溶液PH由大到小的顺序是(填写编号)_________________________________ 2分)由环己烷可制得1, 4 – 环己
2分)由环己烷可制得1, 4 – 环己 二
二 醇,下列有7步反应(其中无机产物都已略去),试回答以下问题:
醇,下列有7步反应(其中无机产物都已略去),试回答以下问题: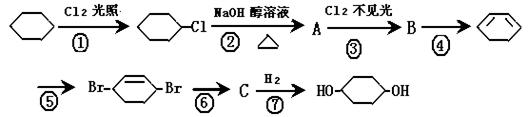
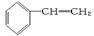 )4种有机物分别在一定条件下与H2充分反应。
)4种有机物分别在一定条件下与H2充分反应。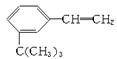 有如下性质:
有如下性质: 粤公网安备 44130202000953号
粤公网安备 44130202000953号