某反应体系中反应物与生成物有: K2SO4、CaSO4、MnSO4、CaC2O4、KMnO4、H2SO4、H2O和一种未知气体X。
(1)已知CaC2O4在反应中失去电子,则该反应的氧化剂是 。
(2)在标准状况下生成11.2LX时,有0.5mol 电子转移,共消耗0.25mol CaC2O4,X的化学式为 。
(3)将氧化剂和还原剂的化学式及其配平后的系数填入下列方框中,并标出电子转移的方向和数目:
|
|
+
(4) 反应中CaC2O4表现 性,发生 反应,生成 产物(选填“氧化”或“还原”),氧化还原反应的本质是 。
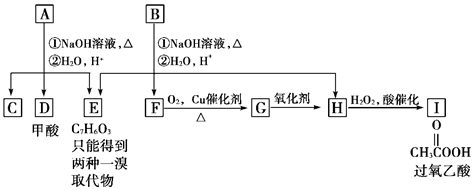
 ,其生产过程如下图,根据下图回答:
,其生产过程如下图,根据下图回答: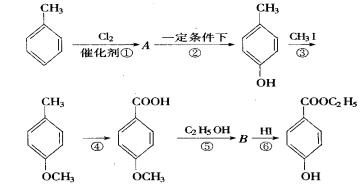
 、一CHO、一COOH、一OH,
、一CHO、一COOH、一OH,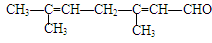
 粤公网安备 44130202000953号
粤公网安备 44130202000953号