BAD是一种紫外线吸收剂,其合成方法如下:
已知:
Ⅰ、B分子中所有H原子的化学环境相同;
Ⅱ、BAD的结构为: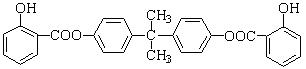 。
。
请回答下列问题:
⑴ A的名称为 。
⑵ F的结构简式为 。F的一些同分异构体能使氯化铁溶液变色,能发生银镜反应,且苯环上的一硝基取代产物有两种。符合上述条件的同分异构体有 种。
⑶ 反应②的化学方程式为 ;反应③在一定条件下能直接进行,其反应类型为 。
⑷ G是一种氨基酸,且羧基和氨基处于苯环的对位。写出G缩聚产物可能的结构简式 (只要求写一种)。
BAD是一种紫外线吸收剂,其合成方法如下:
已知:
Ⅰ、B分子中所有H原子的化学环境相同;
Ⅱ、BAD的结构为: 。
。
请回答下列问题:
⑴ A的名称为 。
⑵ F的结构简式为 。F的一些同分异构体能使氯化铁溶液变色,能发生银镜反应,且苯环上的一硝基取代产物有两种。符合上述条件的同分异构体有 种。
⑶ 反应②的化学方程式为 ;反应③在一定条件下能直接进行,其反应类型为 。
⑷ G是一种氨基酸,且羧基和氨基处于苯环的对位。写出G缩聚产物可能的结构简式 (只要求写一种)。