常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为;
(2)冰比硫化氢熔点高的原因是,冰分子中氧原子的杂化轨道类型为;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
电离能/kJ·mol-1
|
I1
|
I2
|
I3
|
I4
|
X
|
578
|
1817
|
2745
|
11578
|
Y
|
738
|
1451
|
7733
|
10540
|
Z
|
496
|
4562
|
6912
|
9543
|
元素Y第一电离能大于X的原因是;
(4)融雪剂对环境危害很大,如和路基上的铁等金属形成原电池,加快路面破损。铁元素应用广泛,Fe2+与KCN溶液反应得Fe(CN)2沉淀,KCN过量时沉淀溶解,生成黄血盐,结构如图。
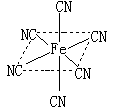
①写出铁元素基态原子价电子的轨道表示式;
②已知CN- 与 N2 结构相似,1 mol CN- 中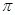 键数目为;
键数目为;