高考化学二轮专题冲刺第6讲 化学反应速率和化学平衡练习卷
无水氯化铝是一种重要的催化剂,工业上由Al2O3制备无水氯化铝的反应为:2Al2O3(s)+6Cl2(g) 4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( )
4AlCl3(g)+3O2(g) ΔH>0 。下列分析错误的是( )
| A.增大反应体系的压强,反应速率可能加快 |
| B.加入碳粉,平衡向右移动,原因是碳与O2反应,降低了生成物的浓度且放出热量 |
| C.电解熔融的Al2O3和AlCl3溶液均能得到单质铝 |
| D.将AlCl3·6H2O在氯化氢气流中加热,也可制得无水氯化铝 |
在容积不变的密闭容器中进行反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( )
| A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 |
| B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响 |
| C.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响 |
| D.图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |
某恒温密闭容器中,可逆反应A(s)B+C(g) ΔH=Q kJ/mol (Q>0)达到平衡。缩小容器体积,重新达到平衡时,C(g)的浓度与缩小体积前的平衡浓度相等。以下分析不正确的是( )
A.产物B的状态只能为固态或液态
B.平衡时,单位时间内n(A)消耗∶n(C)消耗=1∶1
C.保持体积不变,向平衡体系中加入B,平衡可能向逆反应方向移动
D.若开始时向容器中加入1 mol B和1 mol C,达到平衡时放出热量Q
在一个不导热的密闭反应器中,只发生两个反应:
a(g)+b(g)  2c(g) ΔH1<0
2c(g) ΔH1<0
x(g)+3y(g)  2z(g) ΔH2>0
2z(g) ΔH2>0
进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述错误的是( )
| A.等压时,通入惰性气体,c的物质的量不变 |
| B.等压时,通入z气体,反应器中温度升高 |
| C.等容时,通入惰性气体,各反应速率不变 |
| D.等容时,通入z气体,y的物质的量浓度增大 |
将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
| 压强/MPa 体积分数/% 温度/℃ |
1.0 |
2.0 |
3.0 |
| 810 |
54.0 |
a |
b |
| 915 |
c |
75.0 |
d |
| 1 000 |
e |
f |
83.0 |
① b<f ② 915℃、2.0 MPa时E的转化率为60%③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃)
上述①~④中正确的有( )
A.4个 B.3个 C.2个 D.1个
下列说法错误的是( )
A.对于A(s)+2B(g)  3C(g) ΔH>0,若平衡时C的百分含量跟条件X、Y的关系如图①所示,则Y可能表示温度,X可能表示压强,且Y3>Y2>Y1
3C(g) ΔH>0,若平衡时C的百分含量跟条件X、Y的关系如图①所示,则Y可能表示温度,X可能表示压强,且Y3>Y2>Y1
B.已知可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,则图②可表示温度对NO的百分含量的影响
4NO(g)+6H2O(g) ΔH=-1 025 kJ·mol-1。若反应物起始物质的量相同,则图②可表示温度对NO的百分含量的影响
C.已知反应2A(g)  B(?)+2C(?)-Q(Q>0),满足如图③所示的关系,则B、C可能均为气体
B(?)+2C(?)-Q(Q>0),满足如图③所示的关系,则B、C可能均为气体
D.图④是恒温下某化学反应的反应速率随反应时间变化的示意图,则该反应的正反应是一个气体体积增大的反应
有甲、乙两个相同的恒容密闭容器,体积均为0.25 L,在相同温度下均发生可逆反应:X2(g)+3Y2(g)  2XY3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如表所示:
2XY3(g) ΔH=-92.6 kJ·mol-1。实验测得起始、平衡时的有关数据如表所示:
| 容器编号 |
起始时各物质的物质的量/mol |
平衡时体系 能量的变化 |
||
| X2 |
Y2 |
XY3 |
||
| 甲 |
1 |
3 |
0 |
放出热量:23.15 kJ |
| 乙 |
0.9 |
2.7 |
0.2 |
放出热量:Q |
下列叙述错误的是( )
A.若容器甲体积为0.5 L,则平衡时放出的热量小于23.15 kJ
B.容器乙中达平衡时放出的热量Q=23.15 kJ
C.容器甲、乙中反应的平衡常数相等
D.平衡时,两个容器中XY3的体积分数均为1/7
在1.0 L密闭容器中放入0.10 mol A (g),在一定温度进行如下反应:A(g)  B(g)+C(g) ΔH=+85.1 kJ·mol-1
B(g)+C(g) ΔH=+85.1 kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
| 时间t/h |
0 |
1 |
2 |
4 |
8 |
16 |
20 |
25 |
30 |
| 总压强p /100 kPa |
4.91 |
5.58 |
6.32 |
7.31 |
8.54 |
9.50 |
9.52 |
9.53 |
9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为________。
(2)由总压强p和起始压强p0计算反应物A的转化率α(A)的表达式为________________________________________________________________________,平衡时A的转化率为________,列式并计算反应的平衡常数K_______________。
(3)①由总压强p和起始压强p0表示反应体系的总物质的量n总和反应物A的物质的量n(A),n总=________mol,n(A)=________mol。
②下表为反应物A浓度与反应时间的数据,计算a=__________________。
| 反应时间t/h |
0 |
4 |
8 |
16 |
| c(A)/(mol·L-1) |
0.10 |
a |
0.026 |
0.006 5 |
分析该反应中反应物的浓度c(A)变化与时间间隔(Δt)的规律,得出的结论是________,由此规律推出反应在12 h时反应物的浓度c(A)为________mol·L-1。
化学反应4A(s)+3B(g)  2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示正确的是( )
2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示的反应速率其比值是3∶2∶1
C.2 min末的反应速率用B表示是0.3 mol·(L·min)-1
D.2 min内,v正(B)和v逆(C)表示的反应速率的值都是逐渐减小的
可逆反应2SO2(g)+O2(g)2SO3(g),根据下表中的数据判断下列图像错误的是( )
| 压强 转化率 温度 |
p1(MPa) |
p2(MPa) |
| 400℃ |
99.6 |
99.7 |
| 500℃ |
96.9 |
97.8 |

已知2SO2(g)+O2(g)  2SO3(g) ΔH=-a kJ·mol-1(a>0)。恒温恒容下,在10 L的密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0.025 a kJ。下列判断正确的是( )
2SO3(g) ΔH=-a kJ·mol-1(a>0)。恒温恒容下,在10 L的密闭容器中加入0.1 mol SO2和0.05 mol O2,经过2 min达到平衡状态,反应放热0.025 a kJ。下列判断正确的是( )
| A.在2 min内,v(SO2)=0.25 mol·L-1·min-1 |
| B.若再充入0.1 mol SO3,达到平衡后SO3的质量分数会减小 |
| C.在1 min时,c(SO2)+c(SO3)=0.01 mol·L-1 |
| D.若恒温恒压下,在10 L的密闭容器中加入0.1 mol SO2和0.05 mol O2,平衡后反应放热小于0.025a kJ |
将a L NH3通入某恒压的密闭容器中,在一定条件下让其分解,达到平衡后气体体积增大到b L(气体体积在相同条件下测定)。下列说法中正确的是( )
A.平衡后氨气的分解率为 ×100% ×100% |
B.平衡混合气体中H2的体积分数为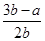 ×100% ×100% |
C.反应前后气体的密度比为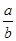 |
D.平衡后气体的平均摩尔质量为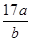 g g |
在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)  2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
| A.容器内密度不随时间变化 |
| B.容器内各物质的浓度不随时间变化 |
| C.容器内X、Y、Z的浓度之比为1∶2∶2 |
| D.单位时间消耗0.1 mol X同时生成0.2 mol Z |
已知反应①:CO(g)+CuO(s)CO2(g)+Cu(s)和反应②:H2(g)+CuO(s)  Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)
Cu(s)+H2O(g)在相同的某温度下的平衡常数分别为K1和K2,该温度下反应③:CO(g)+H2O(g)  CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
CO2(g)+H2(g)的平衡常数为K。则下列说法正确的是( )
A.反应①的平衡常数K1= |
B.反应③的平衡常数K= |
| C.对于反应③,恒容时,温度升高,H2浓度减小,则该反应的焓变为正值 |
| D.对于反应③,恒温恒容下,增大压强,H2浓度一定减小 |
在某温度下,将2 mol A和3 mol B充入一密闭容器中,发生反应:aA(g)+B(g)C(g)+D(g),5 min后达到平衡,已知各物质的平衡浓度的关系为ca(A)·c(B)=c(C)·c(D)。若在温度不变的情况下,将容器的体积扩大为原来的10倍,A的转化率没有发生变化,则B的转化率为( )
A.60% B.40% C.24% D.4%
在100℃时,将0.40 mol NO2气体充入2 L密闭容器中,每隔一段时间对该容器的物质进行测量,得到的数据如下表:
| 时间(s) |
0 |
20 |
40 |
60 |
80 |
| n(NO2)(mol) |
0.40 |
n1 |
0.26 |
n3 |
n4 |
| n(N2O4)(mol) |
0.00 |
0.05 |
n2 |
0.08 |
0.08 |
下列说法中正确的是( )
A.反应开始20 s内NO2的平均反应速率是0.001 mol·L-1·s-1
B.80 s时混合气体的颜色与60 s时颜色相同,比40 s时的颜色深
C.80 s时向容器内加0.32 mol He,同时将容器扩大为4 L,则平衡不移动
D.若起始投料为0.20 mol N2O4,相同条件下达到平衡,则各组分的含量与原平衡相同
(1)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g)+2H2(g)  CH3OH(g)。
CH3OH(g)。
根据题意和所给图像完成下列各题:
①反应达到平衡时,平衡常数表达式K=________。
②升高温度,K值________(填“增大”、“减小”或“不变”)。
(2)一定温度下,将3 mol A气体和1 mol B气体通入一密闭容器中,发生如下反应:3A(g)+B(g)xC(g)。若容器体积固定为2 L,反应2 min时测得剩余0.6 mol B,C的浓度为0.4 mol·L-1。
请填写下列空白:
①x=________。
②平衡混合物中,C的体积分数为50%,则B的转化率是______________。
合成氨工业的核心反应是:N2(g)+3H2(g)  2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
2NH3(g) ΔH=Q kJ·mol-1,能量变化如下图,回答下列问题:
(1)在反应体系中加入催化剂,反应速率增大,E1和E2的变化是:E1________,E2________(填“增大”、“减小”或“不变”)。
(2)在500℃、2×107Pa和催化剂条件下向一密闭容器中充入0.5 mol N2和1.5 mol H2,充分反应后,放出的热量________ 46.2 kJ(填“<”、“>”或“=”)。
(3)关于该反应的下列说法中,正确的是________。
A.ΔH>0,ΔS>0 B.ΔH>0,ΔS<0
C.ΔH<0,ΔS>0 D.ΔH<0,ΔS<0
(4)将一定量的N2(g)和H2(g)放入1 L密闭容器中,在500℃、2×107Pa下达到平衡,测得N2为0.10 mol,H2为0.30 mol,NH3为0.10 mol。计算该条件下达到平衡时H2转化为NH3的转化率________。若升高温度,K值变化________(填“增大”、“减小”或“不变”)。
(5)在上述(4)反应条件的密闭容器中,欲提高合成氨中H2的转化率,下列措施可行的是________(填字母)。
A.向容器中按原比例再充入原料气
B.向容器中再充入惰性气体
C.改变反应的催化剂
D.分离出氨气
2013年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)汽车尾气净化的主要原理为2NO(g)+2CO(g) 2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线如图所示。
据此判断:
①该反应的ΔH________0(填“>”或“<”)
②在T2温度下,0~2 s内的平均反应速率v(N2)=______________________。
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在上图中画出c(CO2)在T1、S2条件下达到平衡过程中的变化曲线。
④若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是________(填代号)。

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染。
例如:CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH1=-867 kJ/mol
2NO2(g)N2O4(g) ΔH2=-56.9 kJ/mol
写出CH4(g)催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式:________________________________________________________________________。
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的
目的。如图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂b表面发生的电极反应式为__________________________。
③常温下,0.1 mol·L-1的HCOONa溶液pH为10,则HCOOH的电离常数Ka=________。




 粤公网安备 44130202000953号
粤公网安备 44130202000953号