2012年鲁科版高中化学必修2 2.2化学反应的快慢和限度练习卷
下图曲线a表示放热反应X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是( )
| A.升高温度 | B.加大X的投入量 | C.加催化剂 | D.增大体积 |
一定条件下,可逆反应2A B+3C,在下列四种状态中处于平衡状态的是( )
B+3C,在下列四种状态中处于平衡状态的是( )
| 正反应速率 |
逆反应速率 |
| A.v(A)=2mol/(L·min), |
v(B)=2mol/(L·min) |
| B. v(A)=2mol/(L·min), |
v(C)=2mol/(L·min) |
| C. v(A)=1mol/(L·min), |
v(B)=2mol/(L·min) |
| D. v(A)=1mol/(L·min), |
v(C)=1.5mol/(L·min) |
把100mL6mol/L的H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率而不影响生成H2的总量,可在反应物中加入适量的 ( )
| A.Na2CO3固体 | B.NaOH固体 | C.硫酸钾溶液 | D.水 |
反应4A(s)+3B(g)==2C(g)+D(g),2min后B的浓度减小0.6mol/L。对此反应速率的不正确表示是( )
A.用A表示的反应速率是0.4mol/(L·min)
B.用B、C、D分别表示反应的速率,其比值是3:2:1
C.在2min末的反应速率,用B表示是0.3mol/(L·min)
D.在2min内的反应速率,用D表示是0.1mol/(L·min)
将ag块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如图中的实线所示,在相同的条件下,将bg(a>b)粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线(图中虚线所示)正确的是( )

在容积固定的2L密闭容器中,一定条件下,发生如下反应:x(g)+2Y(g)==nZ(g),反应过程中各物质的物质的量与时间的关系如下图所示,以下有关叙述中正确的是( )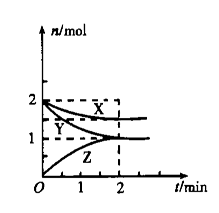
①n=1②n=2③反应开始至2min时,Y的转化率为50%④反应开始至平衡时, v (X)为0.75mol/(L· min)⑤X的平衡浓度为0.75mol/L⑥达平衡时容器内的压强是开始时的0.875倍
| A.②③⑤⑥ | B.②④⑤ | C.②③④⑥ | D.①③④⑥ |
在一定条件下,A2(g)+B2(g) 2AB(g)达到平衡的标志是 ( )
2AB(g)达到平衡的标志是 ( )
| A.单位时间生成nmolA2的同时生成nmolAB |
| B.容器内的总压强不随时间变化 |
| C.单位时间生成2nmolAB的同时生成nmolB2 |
| D.单位时间内生成nmolA2的同时生成nmolB2 |
可逆反应N2+3H2 2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是 ( )
2NH3的正、逆反应速率可用各反应物或生成物浓度的变化来表示。下列各关系中能说明反应已达到平衡状态的是 ( )
| A.3v正(N2)= v正(H2) | B.v正(N2)= v逆(NH3) |
| C.2v正(H2)= 3v逆(NH3) | D.v正(N2)= 3v逆(H2) |
反应A(g)+3B(g)  2C(g)(正反应为放热反应),达平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
2C(g)(正反应为放热反应),达平衡后,将气体混合物的温度降低,下列叙述中正确的是( )
| A.正反应速率加大,逆反应速率变小,平衡向正反应方向移动 |
| B.正反应速率变小,逆反应速率加大,平衡向逆反应方向移动, |
| C.正反应速率和逆反应速率都变小,平衡向正反应方向移动 |
| D.正反应速率和逆反应速率都变小,平衡向逆反应方向移动 |
3A(g)  3B(?)+C(?)(正反应为吸热反应).随着温度的升高,气体的平均相对分子质量有变小趋势,则下列判断正确的是( )
3B(?)+C(?)(正反应为吸热反应).随着温度的升高,气体的平均相对分子质量有变小趋势,则下列判断正确的是( )
| A.B和c可能都是固体 | B.B和C一定都是气体 |
| C.若C为固体,则B一定是气体 | D.B和c可能都是气体 |
将4molA气体和2molB气体在2L的容器中混合,并在一定条件下发生如下反应2A(g)+B(g)  2C(g),若2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是( )
2C(g),若2s后测得C的浓度为0.6mol/L,现有下列几种说法,其中正确的是( )
①用物质A表示的平均反应速率为0.3mol/(L·s)
②用物质B表示的平均反应速率为0.6mol/(L·s)
③2s时物质A的转化率为70%
④2s时物质B的浓度为0.7mol/L
| A.①③ | B.①④ | C.②③ | D.③④ |
将氮气、氢气的混合气体分别充入甲、乙、丙三个容器中进行合成氨反应,经过一段时间后,反应速率为:甲:v (H2)=3mol/(L· min);乙:v (N2) =2mol/(L·min);丙: v (NH3)= 1mol/(L·min),则这段时间内三个容器中反应速率由大到小的顺序是 。
已知反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了4.5mol,试计算分别用NH3、O2、NO、H2O四种不同物质表示的该反应的反应速率。
盐酸与碳酸钙反应时,下列措施能使最初的反应速率明显加快的是( )
| A.增加碳酸钙的量 | B.盐酸的用量增加一倍 |
| C.盐酸的用量减半、浓度加倍 | D.温度升高 |
对某一可逆反应来说,使用催化剂的作用是( )
| A.提高反应物的平衡转化率 |
| B.以同等程度改变正逆反应的速率 |
| C.增大正反应速率,减小逆反应速率 |
| D.改变平衡混合物的组成 |
一定条件下,在密闭容器中,能表示反应X(g)+2Y(g) 2Z(g)一定达到化学平衡状态的是( )
2Z(g)一定达到化学平衡状态的是( )
①X、Y、Z的物质的量之比为l:2:2
②X、Y、Z的浓度不再发生变化
③容器中的压强不再发生变化
④单位时间内生成nmolZ,同时生成2nmolY
| A.①② | B.①④ | C.②③ | D.③④ |
二氧化氮存在下列平衡:2N02(g) N204(g),△H<0,在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
N204(g),△H<0,在测定NO2的相对分子质量时,下列条件中较为适宜的是( )
| A.温度130℃、压强3.03×105Pa |
| B.温度25℃、压强1.01×105Pa |
| C.温度130℃、压强5.05×104Pa |
| D.温度0℃、压强5.05×105Pa |
反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,NH3减少了0.12mol,则平均每秒钟浓度变化是
①NO: ,②O2: 。
已知反应A+3B==2C+D,在30s内A的浓度减小了0.5mol/L,则此段时间内以B的浓度变化表示的反应速率为 mol/(L· min) ,以C的浓度变化表示的反应速率为 mol/(L·min) 。
反应A+3B 2C+2D在四种不同情况下的反应速率分别为:
2C+2D在四种不同情况下的反应速率分别为:
① =0.15mol/(L·min) ②
=0.15mol/(L·min) ② =0.01mol/(L·s)
=0.01mol/(L·s)
③ =0.40mol/(L·min) ④
=0.40mol/(L·min) ④ =0.45mol/(L·min),
=0.45mol/(L·min),
该反应进行的快慢顺序为(填序号) 。
同质量的锌与盐酸反应,欲使反应速率增大,选用的反应条件正确的组合是 。反应条件:①锌粒;②锌片;③锌粉;④5%盐酸;⑤10%盐酸;⑥15%盐酸;⑦加热;⑧用冷水冷却;⑨不断震荡;⑩迅速混合后静置。欲使反应速率进一步增大,可采取的措施是(列举一条) 。
“碘钟”实验中,3I-+S2O82-=I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
| 实验编号 |
① |
② |
③ |
④ |
⑤ |
| c(I-)/mol·L- |
0.040 |
0.080 |
0.080 |
0.160 |
0.120 |
| c(SO42-)/mol·L- |
0.040 |
0.040 |
0.080 |
0.020 |
0.040 |
| t /s |
88.0 |
44.0 |
22.0 |
44.0 |
t2 |
回答下列问题:
(1)该实验的目的是 。
(2)显色时间t2= 。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为 (填字母)
A <22.0s B 22.0~44.0s C >44.0s D 数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是 。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号