河南省郑州智林学校高二下学期阶段测试2化学卷
生活中遇到的下列问题,不涉及化学变化的是
| A.普通鸭蛋制成松花蛋 |
| B.用酒精可擦去圆珠笔油渍 |
| C.蜂蚁蜇咬初涂擦氨水可止痒减痛 |
| D.烹鱼时加少量食醋和白酒可除腥味 |
用硫酸做催化剂使淀粉水解,为测得淀粉水解是否完全,下列试剂最适合选用的是
| A.新制氢氧化铜 | B.银氨溶液 |
| C.氢氧化钠溶液 | D.碘水 |
验证某有机物属于烃的含氧衍生物,应完成的实验内容是
| A.验证它完全燃烧后产物只有H2O和CO2 |
| B.测定其燃烧产物中H2O和CO2物质的量的比值 |
| C.测定完全燃烧时消耗有机物与生成的CO2、H2O的物质的量之比 |
| D.测定该试样的质量及其试样完全燃烧后生成CO2的质量和H2O的质量 |
已知丙烷的二氯代物有四种同分异构体,则其六氯代物的异构体数目为
| A.两种 | B.三种 | C.四种 | D.五种 |
下列说法不正确的是
| A.甘氨酸和丙氨酸缩合最多可以形成四种二肽 |
| B.液态油酸甘油酯加氢转化为固态硬脂酸甘油酯 |
| C.用75%的乙醇消毒,是使细菌、病毒蛋白质盐析而死亡 |
| D.等物质的量苯酚和甲醛在碱的催化下加热反应形成网状酚醛树脂可作绝缘材料 |
下列关于降解包装材料聚乳酸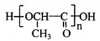 的说法中,正确的是
的说法中,正确的是
| A.聚乳酸是一种纯净物 |
| B.其单体是CH3CH(OH)COOH |
| C.通过乳酸制备聚乳酸的反应是加聚反应[ |
| D.从乳酸制备聚乳酸原子利用率为100% |
乙醇分子中各化学键如下图所示,乙醇在以下各种反应中对应断键说明不正确的是
| A.和金属钠作用时,键①断裂 |
| B.和乙酸、浓硫酸共热时,键①断裂 |
| C.和浓硫酸共热至170℃时,键②和④断裂 |
| D.在铜催化下和氧气加热反应时,键①和③断裂 |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是
| |
混合物 |
试剂 |
分离方法 |
| A |
苯(苯酚)[ |
溴水 |
分液 |
| B |
乙醇(水) |
钠 |
蒸馏 |
| C |
溴苯(溴) |
氢氧化钠溶液 |
分液 |
| D |
乙酸乙酯(乙酸)[] |
饱和碳酸钠溶液 |
过滤 |
用一种试剂即可鉴别苯酚溶液、1-己烯、乙醇、苯,这种试剂是
| A.溴水 | B.FeCl3溶液 | C.NaOH溶液 | D.四氯化碳 |
相同物质的量的下列物质,在空气中充分燃烧消耗氧气最多的是
| A.C6H12 | B.C6H6O6 | C.C5H11COOH | D.C6H5OH |
下列各离子可以大量共存、加入括号中的试剂,可以形成无色澄清溶液的是( )
| A.Mg2+、Cu2+、NO3-(稀盐酸) | B.Ag+、Al3+、NO3-(氨水) |
| C.Al3+、K+、SO42-(NaOH溶液) | D.Ba2+、Na+、SO32+(稀HNO3) |
以惰性电极电解溶液,若阳极上产生气体的物质的量为0.01,则阴极上析出的铜的质量为()
| A. | 0.64 | B. | 1.28g | C. | 2.56g | D. | 5.12g |
已知:2H2(g)+ O2(g)=2H2O(l) ;ΔH=" -571.6KJ·" mol-1
CH4(g)+ 2O2(g)=CO2(g)+2H2O(l) ;ΔH=" -890KJ·" mol-1
现有H2与CH4的混合气体112L(标准状况),使其完全燃烧生成CO2和H2O(l),若实验测得反应放热3695KJ,则原混合气体中H2与CH4的物质的量之比是( )
| A.1∶1 | B.1∶3 | C.1∶4 | D.2∶3 |
下列各项中顺序排列错误的是( )
| A.热稳定性:PH3>H2S>HCl>NH3 |
| B.熔点:石英>食盐>白磷>冰 |
| C.作用力大小:共价键>氢键>范德华力 |
| D.分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
在25℃时,用铂电极电解一定量的Na2SO4饱和溶液,一段时间后,阳极析出amol气体,同时溶液中析出bg Na2SO4·10H2O,如果在这一过程中温度不变,则此时Na2SO4溶液中溶质的质量分数为( )
| A.(71/161)×100℅ | B.〔71b/161(18a+b)〕×100℅ |
| C.〔b/(18a+b)〕×100℅ | D.〔71b/161(36a+b)〕×100℅ |
已知Zn2+的4s轨道和4p轨道可以形成sp3型杂化轨道,那么[ZnCl4]2—的空间构型为
| A.直线形 | B.平面正方形 | C.正四面体形 | D.正八面体形 |
某物质的晶体晶胞中含有A、B、C三种元素,其晶胞如图所示(其中前后两面面心中的B元素的原子未能画出)。晶体中A、B、C的原子个数比为
A.1∶3∶1 B.2∶3∶1 C.2∶2∶1 D.1∶3∶3
下列分子中的σ键是由一个原子的s轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成的是
| A.H2 | B.HCl | C.Cl2 | D.F2 |
(9分).邻羟基苯甲酸(俗名水杨酸)其结构简式为 :
:
(1).水杨酸既可以看成是__________类物质,同时也可以看成是_____________类物质。
(2).将其与_______________溶液作用生成物的化学式为C7H5O3Na
将其与_______________溶液作用生成物的化学式为C7H4O3Na2
(3).水杨酸的不同类同分异构体中,属于酚类且也具有苯环的化合物的结构简式为______________,它还可看成是__________类物质。
(4).比水杨酸多一个CH2原子团,且与水杨酸属于同系物的取代基数目不同的两类物质的结构简式分别为___________________ ________________
(5).比水杨酸多一个CH2原子团,且与水杨酸不属于同系物的两类物质的结构简式分别为_________________________________________
.如下图所示:淀粉水解可产生某有机化合物A,A在不同的氧化剂作用下,可以生成B(C6H12O7)或C(C6H10O8),B和C都不能发生银镜反应。A、B、C都可以被强还原剂还原成为D(C6H14O6)。B脱水可得到五元环的酯类化合物E或六元环的酯类化合物F。
已知,相关物质被氧化的难易次序是:
RCHO最易, R—CH2OH次之, 最难。
最难。
(1)请写出C、D的结构简式:C:__________D:______________________
(2)请写出下列反应的化学方程式
①淀粉水解A:__________________________________________
②A发生银镜反应:______________________________________
③B → F:_____________________________________________
(12分)实验室用加热l-丁醇、溴化钠和浓H2SO4的混合物的方法来制备1-溴丁烷时,还会有烯、醚等副产物生成。反应结束后将反应混合物蒸馏,分离得到1—溴丁烷,已知相关有机物的性质如下:
| |
熔点/oC |
沸点/oC |
| 1-丁醇 |
—89.53 |
—117.25 |
| 1-溴丁烷 |
—112.4 |
—101.6 |
| 丁醚 |
—95.3 |
—142.4 |
| 1-丁烯 |
—185.3 |
—6.5 |

A B C D
⑴制备1-溴丁烷的装置应选用上图中的_______(填序号)。反应加热时的温度不宜超过
100℃,理由是_________________________。
⑵制备操作中,加入的浓硫酸必需进行稀释,其目的是 。(填字母)
a.减少副产物烯和醚的生成 b.减少Br2的生成
c.减少HBr的挥发 d.水是反应的催化剂 。
⑶反应结束后,将反应混合物中1-溴丁烷分离出来,应选用的装置是______。该操作应控制的温度(t)范围是_______________。
⑷欲除去溴代烷中的少量杂质Br2,下列物质中最适合的是 。(填字母)
a.NaI b.NaOH c.NaHSO3 d.KCl
(12分) 通过粮食发酵可获得某含氧有机化合物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数为13.0%。
(1)X的分子式是________________;
(2)X与金属钠反应放出氢气,反应的化学方程式是
________________________________________________(有机物用结构简式表达);
(3)X与空气中的氧气在铜或银催化下反应生成Y,Y的结构简式是_________________;
(4)X与高锰酸钾酸性溶液反应可生成Z。在加热和浓硫酸作用下,X与Z反应可生成一种有香味的物质W,若184 g X和120 g Z反应能生成106 g W,计算该反应的产率。(要求写出计算过程)
已知磷酸分子 中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是
中的三个氢原子都可以跟重水分子(D2O)中的D原子发生氢交换,又知次磷酸(H3PO2)也可跟D2O进行氢交换,但次磷酸钠(NaH2PO2)却不再能跟D2O发生氢交换,由此可推断出H3PO2的分子结构是












 粤公网安备 44130202000953号
粤公网安备 44130202000953号