(7分).化合物C是医用功能高分子材料,可由化合物A(C4H8O3)制得,如下图所示,B和D互为同分异构体。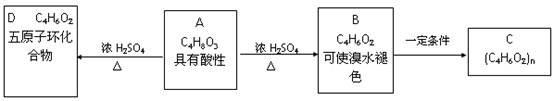
试写出下列反应的化学方程式
A→B
B→C
试写出下列反应的反应类型
A→B B→C A→D
(7分).化合物C是医用功能高分子材料,可由化合物A(C4H8O3)制得,如下图所示,B和D互为同分异构体。
试写出下列反应的化学方程式
A→B
B→C
试写出下列反应的反应类型
A→B B→C A→D