2010年高考化学试题分项专题八 化学反应速率和化学平衡
下列各表述与示意图一致的是

| A. | 图①表示25 时,用0.1 盐酸滴定20 0.1 溶液,溶液的 随加入酸体积的变化 |
| B. |
图②中曲线表示反应
 ;
正、逆反应的平衡常数K随温度的变化
;
正、逆反应的平衡常数K随温度的变化
|
| C. | 图③表示10 0.01 酸性溶液与过量的0.1 溶液混合时, 随时间的变化 |
| D. | 图④中 曲线分别表示反应 ; 使用和未使用催化剂时,反应过程中的能量变化 |
二甲醚是一种重要的清洁燃料,也可替代氟利昂作制冷剂等,对臭氧层无破坏作用。工业上可利用煤的气化产物(水煤气)合成二甲醚。
请回答下列问题:
⑴ 煤的气化的主要化学反应方程式为:。
⑵ 煤的气化过程中产生的有害气体用溶液吸收,生成两种酸式盐,该反应的化 学方程式为:。
学方程式为:。
⑶ 利用水煤气合成二甲醚的三步反应如下:
① 
② 
③ 
总反应: =;
=;
一定条件下的密闭容器中,该总反应达到平衡,要提高的转化率,可以采取的措施是(填字母代号)。
a.高温高压 b.加入催化剂 c.减少CO2的浓度
d.增加的浓度 e.分离出二甲醚
⑷ 已知反应② 某温度下的平衡常数为400 。此温度下,在密闭容器中加入,反应到某时刻测得各组分的浓度如
某温度下的平衡常数为400 。此温度下,在密闭容器中加入,反应到某时刻测得各组分的浓度如 下:
下:
| 物质 |
|||
| 浓度/() |
0.44 |
0.6 |
0.6 |
① 比较此时正、逆反应速率的大小:(填">"、"<"或"=")。
② 若加入后,经10 反应达到平衡,此时() =;该时间内反应速率() =。
在溶液中,反映分别在三种不同实验条件下进行,它们的起始浓度均为、及。反映物的浓度随时间的变化如下图所示。
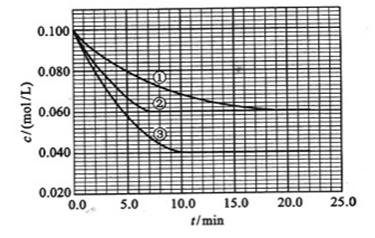

请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:
②;
③;
(2)实验②平衡时的转化率为;实验③平衡时的浓度为;
(3)该反应的>0,判断其理由是;
(4)该反应进行到4.0时的平均反应速度率:
实验②:=;
实验③:=。
低温脱硝技术可用于处理废气中的氮氧化物,发生的化学反应为:
在恒容的密闭容器中,下列有关说法正确的是()
| A. | 平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| B. | 平衡时,其他条件不变,增加 的浓度,废气中氮氧化物的转化率减小 |
| C. | 单位时间内消耗 和 的物质的量比为1:2时,反应达到平衡 |
| D. | 其他条件不变,使用高效催化剂,废气中氮氧化物的转化率增大 |
下列说法不正确的是
| A. | 铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B. | 常温下,反应 不能自发进行,则该反应的 |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率 |
| D. | 相同条件下,溶液中 、 、 的氧化性依次减弱 |
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知 )

下列说法正确的是
| A. | B. | C. | D. |
下表列出了3种燃煤烟气脱硫方法的原理。

(1)方法Ⅰ中氨水吸收燃煤烟气中的化学反应为:


能提高燃煤烟气中去除率的措施有(填字母)。
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D . 通入空气使转化为
. 通入空气使转化为
采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的,原因是(用离子方程式表示)。
(2)方法Ⅱ重要发生了下列反应:




与反应生成的热化学方程式为。
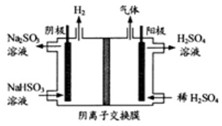
(3)方法Ⅲ中用惰性电极电解溶液的装置如上图所示。阳极区放出气体的成分为。(填化学式)
据报道,在300℃、70下由二氧化碳和氢气合成乙醇已成为现实。下列叙述错误的是
| A. | 使用 催化剂可大大提高生产效率 |
| B. | 反应需在300℃进行可推测该反应是吸热反应 |
| C. | 充入大量 气体可提高 的转化率 |
| D. | 从平衡混合气体中分离出 和 可提高 和 的利用率 |
接触法制硫酸工艺中,其主反应在并有催化剂存在下进行:
1)该反应所用的催化剂是(填写化合物名称),该反应时的平衡常数时的平衡常数(填"大于"、"小于"或"等于").
2)该热化学反应方程式的意义是.
3)达到化学平衡状态的是
a. b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化 d.容器中气体的分子总数不随时间而变化
4)在一个固定容积为5L的密闭容器中充入和,半分钟后达到平衡,测得容器中含,则:若继续通入和,则平衡移动(填"向正反应方向"、"向逆反应方向" 或"不"),再次达到平衡后,mol<<mol。
下列有关化学研究的正确说法是()
| A. | 同时改变两个变量来研究反应速率的变化,能更快得出有关规律 |
| B. | 对于同一个化学反应,无论是一步完成还是分几步完成,其反应的焓变相同 |
| C. | 依据丁达尔现象可将分散素分为溶液、胶体与浊液 |
| D. | 从 、 、 、 酸性递增的事实,推出 、 、 、 的非金属性递增的规律 |
化合物在一定波长的光照射下发生分解反应,反应物浓度

随反应时间变化如右图所示,计算反应4~8间的平均反应速率和推测反应16时反应物的浓度,结果应是
| A. |
2.5和2.0 |
| B. |
2.5和2.5 |
| C. |
3.0和3.0 |
| D. |
5.0和3.0 |
、、、、是原子序数依次增大的短周期主族元素,、在周期表中的相对位置如右表;元素最低负化合价的绝对值与其原子最外层电子数相等;是地壳中含量最多的金属元素。
(1)的离子结构示意图为;元素在周期表中位于第族。
(2)和氢组成的化合物分子有6个原子,其结构简式为。
(3)和形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为
(4)的最简单气态氢化物甲的水溶液显碱性。
①在微电子工业中,甲的水溶液可作刻蚀剂的清除剂,所发生反应的产物不污染环境,其化学方程式为。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(>0)并达平衡后,仅改变下表中反应条件,该平衡体系中随递增递减的是(选填序号)。
| 选项 |
||||
| 温度 |
温度 |
加入的物质的量 |
加入甲的物质的量 |
|
| 甲的物质的量 |
平衡常数K |
甲的转化率 |
生成物物质的量总和 |
(5)由、形成的液态化合物0.2在中完全燃烧,生成两种气态氧化物,298时放出热量215。 该反应的热化学方程式为。
硼酸在食品、医药领域应用广泛。
(1)请完成气体与水反应的化学方程式:+ = +。
(2)在其他条件相同时,反应+ +中,3的转化率在不同温度下随反应时间的变化见图12,由此图可得出:
+中,3的转化率在不同温度下随反应时间的变化见图12,由此图可得出:

①温度对应该反应的反应速率和平衡移动的影响是_
②该反应的0(填"<"、"="或">").
(3)溶液中存在如下反应:
()+() -( )++()已知0.70 -1 溶液中,上述反应于298达到平衡时,(+)="2." 0 × 10-5-1,()≈(),水的电离可忽略不计,求此温度下该反应的平衡常数()的平衡浓度不列入的表达式中,计算结果保留两位有效数字)
-( )++()已知0.70 -1 溶液中,上述反应于298达到平衡时,(+)="2." 0 × 10-5-1,()≈(),水的电离可忽略不计,求此温度下该反应的平衡常数()的平衡浓度不列入的表达式中,计算结果保留两位有效数字)
硫--碘循环分解水制氢主要涉及以下反应
I
Ⅱ
Ⅲ
(1)分析上述反应,下列判断正确的是
a.反应Ⅲ易在常温下进行 b.反应I中氧化性比强
c.循环过程中需补充 d.循环过程中产生1的同时产生1
(2)一定温度下,向1密闭容器中加入1 ,发生反应Ⅱ,物质的量随时间的变化如图所示。

0-2已见分晓的平均反应速率=,该温度下,的平衡常数=。
相同温度下,若开始加入的物质的量是原来的2倍,则是原来的2倍。
a.平衡常数 b.的平衡浓度 c.达到平衡的时间 d.平衡时的体积分数
(3)实验室用和稀硫酸制,反应时候溶液中水的电离平衡移动(填"向左"或"向右"或"不");若加入少量下列试剂中的,产生的速率将增大。
A. B. C. D.
(4)以为燃料可制作氢氧燃料电池。已知
某氢氧燃料电池释放228.8电能时,生成1液态水,该电池的能量转化率为。
高炉炼铁过程中发生的主要反应为
已知该反应在不同温度下的平衡 常数如下:
常数如下:

请回答下列问题:
(1)该反应的平衡常数表达式=,0(填">"、"<"或"=");
(2)在一个容积为10的密闭容器中,1000℃时加入、、、各1.0 ,反应经过l0后达到平衡。求该时间范围内反应的平均反应速率=、的平衡转化率=:
(3)欲提高(2)中的平衡转化率,可采取的措施是。
A.减少的量
B.增加的量
C. 移出部分
D.提高反应温度
E.减小容器的容积
F.加入合适的催化剂
Ⅰ固硫剂是把煤燃烧时生成的二氧化硫以盐的形式固定在炉渣中的物质,可减少二氧化硫对大气的污染。下列物质中可用做固硫剂的有
| A. | B. | C. | D. |
Ⅱ以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:

请回答下列问题:
(1)在炉气制造中,生成的化学方程式为;
(2)炉气精制的作用是将含的炉气、及干燥,如果炉气不经过精制,对催化氧化的影响是 :

(3)精制炉气(含体积分数为7%、为ll%、为82%)中平衡转化率与温度及压强关系如下图所示。在实际生产中,催化氧化反应的条件选择常压、450℃;左右(对应图中点),而没有选择转化率更高的或点对应的反应条件,其原因分别是、;
(4)在催化氧化设备中设置热交换器的目的是、,从而充分利用能源。
反应
 达到平衡时。
的体积分数
与反应条件的关系如图所示。其中:表示反应开始时
的物质的量之比。下列说法正确的是
达到平衡时。
的体积分数
与反应条件的关系如图所示。其中:表示反应开始时
的物质的量之比。下列说法正确的是

| A. | 同温同压 时,加入催化剂,平衡时 的体积分数增加 |
| B. | 同压同 时,升高温度,平衡时 的体积分数增加 |
| C. | 同温同 时,增加压强,平衡时 的体积分数增加 |
| D. | 同温同压时,增加 ,平衡时 的体积分数增加。 |
当反应达到平衡时,下列措施:①升温②恒压通入惰性气体,③增加的浓度④减压⑤加催化剂⑥恒容通入惰性气体;能提高转化率的是( )
| A. | ①②④ | B. | ①④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
钒()及其化合物广泛应用于工业催化、新材料和新能源等领域.
(1)是接触法制硫酸的催化剂.
①一定条件下,与空气反映t 后,和物质的量浓度分别为 和 , 则起始物质的量浓度为mol/L ;生成的化学反应速率为 .
②工业制硫酸,尾气用吸收.
(2)全钒液流储能电池是利用不同价态离子对的氧化还原反应来实现化学能和电能相互转化的装置,其原理如题29图所示.

①当左槽溶液逐渐由黄变蓝,其电极反应式为
②充电过程中,右槽溶液颜色逐渐由色变为色.
③放电过程中氢离子的作用是和;充电时若转移的电子数为3.01 1023个,左槽溶液中的变化量为.
1023个,左槽溶液中的变化量为.
物质有下图所示转化关系(部分反应物、生成物没有列出)。其中为某金属矿的主要成分,经过一系列反应可得到和。单质可与的浓溶液发生反应,为砖红色沉淀。
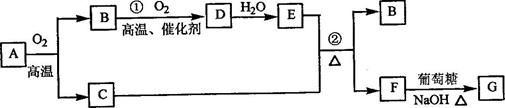
请回答下列问题:
(1)写出下列物质的化学式:
(2)利用电解可提纯物质,在该电解反应中阳极物质是
(3)反应②的化学方程式是
(4)将0.23和0.11氧气放入容积为1的密闭容器中,发生反应①,在一定温度下,反应达到平衡,得到0.12 ,则反应的平衡常数
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的化学方程式有
(2)硫酸铜溶液可以加快氢气生成速率的原因是
(3)实验室中现有、、、等4种溶液,可与实验中溶液起相似作用的是
(4)要加快上述实验中气体产生的速率,还可采取的措施有
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 |
||||||
| 4 | 30 |
1 |
2 |
3 |
4 |
5 |
| 饱和溶液/ | 0 |
0.5 |
2.5 |
5 |
6 |
20 |
| 7 |
8 |
9 |
10 |
10 |
0 |
①请完成此实验设计,其中:1=
②反应一段时间后,实验中的金属呈
③该同学最后得出的结论为:当加入少量溶液时,生成氢气的速率会大大提高。但当加入的溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
 粤公网安备 44130202000953号
粤公网安备 44130202000953号