2015年全国统一高考理综试卷(浙江卷)化学部分
下列说法不正确的是( )
下列说法正确的是( )
| A. | 为测定新制氯水的 ,用玻璃棒蘸取液体滴在 试纸上,与标准比色卡对照即可 |
| B. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 |
| C. | 在未知溶液中滴加 溶液出现白色沉淀,加稀硝酸,沉淀不溶解,说明该未知溶液中存在 或 |
| D. | 提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法 |
下表为元素周期表的一部分,其中、、、为短周期元素,元素的核电荷数为元素的2倍。下列说法正确的是()
| A. | 、 、 元素的原子半径及它们的气态氢化物的热稳定性均依次递增 |
| B. | 、 、 元素在自然界中均不能以游离态存在,它们的最高价氧化物的水化物的酸性依次递增 |
| C. | 晶体熔化、液态 气化均需克服分子间作用力 |
| D. | 根据元素周期律,可以推测 元素的单质具有半导体特性, 具有氧化性和还原性 |
下列说法不正确的是( )
| A. | 己烷有4种同分异构体,它们的熔点、沸点各不相同 |
| B. | 在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 |
| C. | 油脂皂化反应得到高级脂肪酸盐与甘油 |
| D. |
聚合物
 可由单体
和
加聚制得 可由单体
和
加聚制得
|
在固态金属氧化物电解池中,高温共电解混合气体制备和是一种新的能源利用方式,基本原理如图所示。下列说法不正确的是

阴极的反应式是:
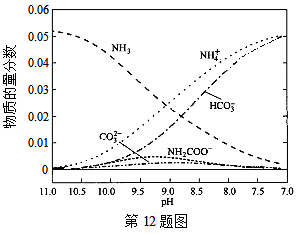
40℃时,在氨-水体系中不断通入,各种离子的变化趋势如下图所示。下列说法不正确的是( )
某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为、、,不考虑其他杂质)制取七水合硫酸亚铁(),设计了如下流程:

下列说法不正确的是()
| A. | 溶解烧渣选用足量硫酸,试剂 选用铁粉 |
| B. | 固体1中一定含有 ,控制pH是为了使 转化为 ,进入固体2 |
| C. | 从溶液2得到 产品的过程中,须控制条件防止其氧化和分解 |
| D. | 若改变方案,在溶液1中直接加 至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到 |
化合物是一种香料,可采用乙烯与甲苯为主要原料,按下列路线合成:

已知: ;+
;+
请回答:
(1)中官能团的名称是
(2)的化学方程式
(3)的结构简式
(4)对于化合物,下列说法正确的是
(5)下列化合物中属于F的同分异构体的是
。
Ⅰ.请回答:
(1)的电子式
(2)镁燃烧不能用灭火,用化学方程式表示其理由
(3)在沉淀中加入KBr溶液,白色沉淀转化为淡黄色沉淀,写出反应的离子方程式
(4)完成以下氧化还原反应的离子方程式:
(___)+(___)+____=(___)+(___)↑+
Ⅱ.化合物甲和都是重要的还原剂。一定条件下金属钠和反应生成甲。甲与水反应可产生,甲与反应可得到。将4.80g甲加热至完全分解,得到金属钠和2.24 L(已折算成标准状况)的。
请推测并回答:
(1)甲的化学式
(2)甲与反应得到的化学方程式
(3)与水发生氧化还原反应的化学方程式
(4)甲在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为),脱锈过程发生反应的化学方程式
(5)某同学认为:用惰性气体赶尽反应体系中的空气,将铁和盐酸反应后的气体经浓硫酸干燥,再与金属钠反应,得到固体物质即为纯净的甲;取该固体物质与水反应,若能产生,即可证明得到的甲一定是纯净的。
判断该同学设想的制备和验纯方法的合理性并说明理由
(15分)乙苯催化脱氢制苯乙烯反应:

(1)已知:
| 化学键 |
||||
| 键能/ | 412 |
348 |
612 |
436 |
计算上述反应的=
(2)维持体系总压强恒定,在温度时,物质的量为、体积为的乙苯蒸汽发生催化脱氢反应。已知乙苯的平衡转化率为,则在该温度下反应的平衡常数=
(3)工业上,通常在乙苯蒸气中掺混水蒸气(原料气中乙苯和水蒸气的物质的量之比为1︰9),控制反应温度600℃,并保持体系总压为常压的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了以外的产物中苯乙烯的物质的量分数)示意图如下:

①掺入水蒸气能提高乙苯的平衡转化率,解释说明该事实
②控制反应温度为600℃的理由是
(4)某研究机构用代替水蒸气开发了绿色化学合成工艺--乙苯-二氧化碳耦合催化脱氢制苯乙烯。保持常压和原料气比例不变,与掺水蒸汽工艺相比,在相同的生产效率下,可降低操作温度;该工艺中还能够发生反应:,。新工艺的特点有
① 与反应,使乙苯脱氢反应的化学平衡右移
② 不用高温水蒸气,可降低能量消耗
③ 有利于减少积炭
④ 有利于资源利用
某学习小组按如下实验流程探究海带中碘含量的测定和碘的制取。
实验(一) 碘含量的测定

取0.0100标准溶液装入滴定管,取100.00海带浸取原液至滴定池,用电势滴定法测定碘含量。测得的电动势() 反映溶液中的变化,部分数据如下表:
| 15.00 |
19.00 |
19.80 |
19.98 |
20.00 |
20.02 |
21.00 |
23.00 |
25.00 |
|
| -225 |
-200 |
-150 |
-100 |
50.0 |
175 |
275 |
300 |
325 |
实验(二) 碘的制取
另制海带浸取原液,甲、乙两种实验方案如下:

已知:。
请回答:
(1)实验(一) 中的仪器名称:仪器
(2)①根据表中数据绘制滴定曲线:

②该次滴定终点时用去溶液的体积为
(3)①分液漏斗使用前须检漏,检漏方法为
②步骤中,萃取后分液漏斗内观察到的现象是
③下列有关步骤的说法,正确的是
A.应控制溶液的浓度和体积
B.将碘转化成离子进入水层
C.主要是除去海带浸取原液中的有机杂质
D.溶液可以由乙醇代替
④实验(二) 中操作的名称是
(4)方案甲中采用蒸馏不合理,理由是
 粤公网安备 44130202000953号
粤公网安备 44130202000953号