(15分)I、用CH4催化还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)=4NO(g)+ CO2(g)+2H2O(g) △H= 574 kJ·moll
②CH4(g)+4NO(g)=2N2(g)+ CO2(g)+ 2H2O(g) △H= 1160 kJ·moll
③H2O(l)=H2O(g) △H=+44kJ·moll
写出CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式___。
II、开发新能源和三废处理都是可持续发展的重要方面。CO在催化剂作用下可以与H2反应生成甲醇:CO(g)+2H2(g)  CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如图所示。
CH3OH(g)。在密闭容器中充有10 mol CO与20 mol H2,CO的平衡转化率与温度、压强的关系如图所示。
(1)M、N两点平衡状态下,容器中物质的总物质的量之比为:n(M)总:n(N)总= 。
(2)若M、N、Q三点的平衡常数KM、KN、KQ的大小关系为 ;P1 P2 (填“>” 或“<” 或“=”)
III、用MnO2制KMnO4的工艺流程如下图:电解池中两极材料均为碳棒,在中性或酸性溶液中K2MnO4发生歧化反应而变成MnO2和KMnO4。
(1)写出240℃熔融时发生反应的化学方程式 ;投料时必须满足n(KOH):n(MnO2) 。
(2)阳极的电极反应式为 。
(3)B物质是 (填化学式),可以循环使用的物质是 (填化学式)。
 温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.20 mol水蒸气,发生反应:
温度下,在2 L密闭容器中加入纳米级Cu2O并通入0.20 mol水蒸气,发生反应:
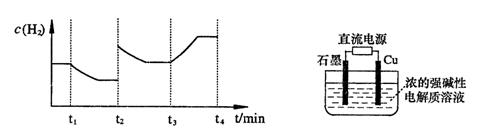
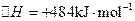 ;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)= ;该温度下,反应的平衡常数表达式K= ;下图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为,t2时改变的条件可能为;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平
;测得20 min时O2的物质的量为0.0016 mol,则前20 min的反应速率v(H2O)= ;该温度下,反应的平衡常数表达式K= ;下图表示在t1时刻达到平衡后,只改变一个条件又达到平衡的不同时段内,H2的浓度随时间变化的情况,则t1时平衡的移动方向为,t2时改变的条件可能为;若以K1、K2、K3分别表示t1时刻起改变条件的三个时间段内的平 衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为;
衡常数,t3时刻没有加入或减少体系中的任何物质,则K1、K2、K3的关系为;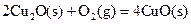 ΔH=-293kJ·mol-1
ΔH=-293kJ·mol-1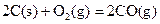 ΔH=-221kJ·mol-1
ΔH=-221kJ·mol-1
 则样品中G的质量分数为: 。
则样品中G的质量分数为: 。 Ⅰ.MnFe2O4的制备:
Ⅰ.MnFe2O4的制备:

 上投入原料Fe(NO3)3和Mn(NO3)2
上投入原料Fe(NO3)3和Mn(NO3)2 O2(g);△H1
O2(g);△H1 。
。
 粤公网安备 44130202000953号
粤公网安备 44130202000953号