从镍氢电池到锂电池,再到钠电池、钾电池,科学家在不断提升电池的性能。
(1)金属失去电子后形成_____离子,锂、钠、钾等原子很容易失去电子变成离子,所以常被用作电池材料。
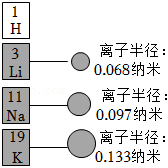
(2)研究表明,半径越大的离子越容易在电池正负极之间移动,充电速度越快。如图是锂、钠、钾三种金属的离子半径大小,电池容量相同的这三种电池,充满电的时间最短的是_____电池。
从镍氢电池到锂电池,再到钠电池、钾电池,科学家在不断提升电池的性能。
(1)金属失去电子后形成_____离子,锂、钠、钾等原子很容易失去电子变成离子,所以常被用作电池材料。
(2)研究表明,半径越大的离子越容易在电池正负极之间移动,充电速度越快。如图是锂、钠、钾三种金属的离子半径大小,电池容量相同的这三种电池,充满电的时间最短的是_____电池。
