请结合如图装置图回答问题:
(1)仪器①的名称是 。
(2)把装置A制取的某气体从装置B的a端通入,B中蜡烛燃烧更旺,则装置A中发生反应的化学方程式是 。 你认为下列哪些物质不能单独作为制取该气体的反应物 (填序号)。
A.NaCl B.KMnO4 C.H2O D.CH4
(3)用装置A、C制取并收集该气体,当装置C中的导管口有气泡 冒出时,再把导管口伸入盛满水的集气瓶里。在收集过程中发现装置A中有大量气泡产生,而装置C中只有少量气泡冒出。你认为实验过程中忘记了什么操作 。
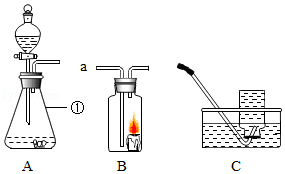
请结合如图装置图回答问题:
(1)仪器①的名称是 。
(2)把装置A制取的某气体从装置B的a端通入,B中蜡烛燃烧更旺,则装置A中发生反应的化学方程式是 。 你认为下列哪些物质不能单独作为制取该气体的反应物 (填序号)。
A.NaCl B.KMnO4 C.H2O D.CH4
(3)用装置A、C制取并收集该气体,当装置C中的导管口有气泡 冒出时,再把导管口伸入盛满水的集气瓶里。在收集过程中发现装置A中有大量气泡产生,而装置C中只有少量气泡冒出。你认为实验过程中忘记了什么操作 。
