中和反应在日常生活中应用广泛,下列是稀盐酸和氢氧化钠溶液反应的微观示意图。回答以下问题: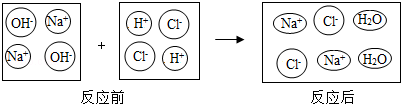
(1)分析图中反应前后没有发生变化的微粒是 、 ;反应的实质是 。
(2)如果规定上述反应后溶液的pH<7,显酸性。请你设计一个实验方案证明溶液显酸性:
实验操作 |
实验现象 |
实验结论 |
①
|
②
|
显酸性 |
中和反应在日常生活中应用广泛,下列是稀盐酸和氢氧化钠溶液反应的微观示意图。回答以下问题:
(1)分析图中反应前后没有发生变化的微粒是 、 ;反应的实质是 。
(2)如果规定上述反应后溶液的pH<7,显酸性。请你设计一个实验方案证明溶液显酸性:
实验操作 |
实验现象 |
实验结论 |
①
|
②
|
显酸性 |