元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:
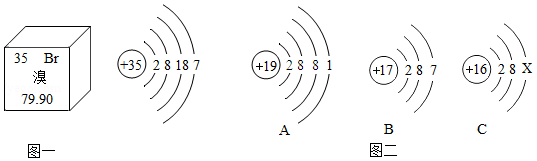
(1)溴的相对原子质量是 。
(2)溴元素的化学性质与图二哪种元素的化学性质相似 (填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为: 。
(4)若图二中C表示离子,则离子符号是 。
元素周期表是学习和研究化学的重要工具。溴元素的相关信息如图一所示,回答下列问题:

(1)溴的相对原子质量是 。
(2)溴元素的化学性质与图二哪种元素的化学性质相似 (填序号)。
(3)溴元素与图二中A元素形成化合物的化学式为: 。
(4)若图二中C表示离子,则离子符号是 。