根据下列图示,回答有关问题。

(1)A图是钾元素在元素周期表中的相关信息,钾元素的相对原子质量是 。
(2)B、C、D、E四种粒子中,具有相对稳定结构的是 (填字母,下同),属于同种元素的是 。
(3)如图是某化学反应的微观示意图。
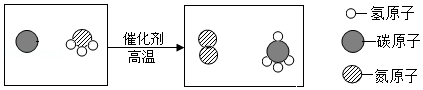
①图中涉及的化合物有 种。
②该反应中生成物的粒子个数比为 。
③反应前后化合价没有发生改变的元素是 。
根据下列图示,回答有关问题。

(1)A图是钾元素在元素周期表中的相关信息,钾元素的相对原子质量是 。
(2)B、C、D、E四种粒子中,具有相对稳定结构的是 (填字母,下同),属于同种元素的是 。
(3)如图是某化学反应的微观示意图。

①图中涉及的化合物有 种。
②该反应中生成物的粒子个数比为 。
③反应前后化合价没有发生改变的元素是 。