某实验小组进行“配制一定溶质质量分数的氯化钠溶液”的实验:
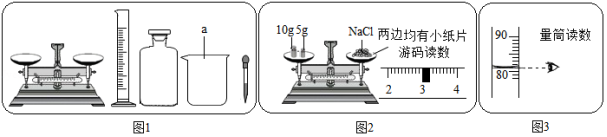
(1)图1中仪器a的名称是 ,图1中还缺少的玻璃仪器是 (填名称)。
(2)小青按图2的操作称取氯化钠,小民发现小青的操作有错误。你认为小青操作中的错误是 。
(3)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为 (水的密度为1g/mL)。
某实验小组进行“配制一定溶质质量分数的氯化钠溶液”的实验:

(1)图1中仪器a的名称是 ,图1中还缺少的玻璃仪器是 (填名称)。
(2)小青按图2的操作称取氯化钠,小民发现小青的操作有错误。你认为小青操作中的错误是 。
(3)小民所取蒸馏水的体积如图3所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为 (水的密度为1g/mL)。