甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)温度为 ℃时,甲、乙、丙种物质的溶解度大小关系为甲=乙>丙.
(2)t3℃时等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最大的是 .
(3)降温结晶过程中甲、乙两物质的溶解度都 (选填“增大”、“减小”或“不变”).
(4)接近饱和的丙溶液,在保持溶质质量分数不变的情况下转变为饱和溶液,可采取的方法是 .
(5)将t3℃时等质量的甲、乙两物质的饱和溶液,同时降温到t1℃,析出甲的质量 乙 (选填“>”“<”或“=”).
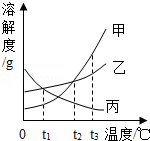
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:
(1)温度为 ℃时,甲、乙、丙种物质的溶解度大小关系为甲=乙>丙.
(2)t3℃时等质量的甲、乙、丙三种物质的饱和溶液中,溶剂质量最大的是 .
(3)降温结晶过程中甲、乙两物质的溶解度都 (选填“增大”、“减小”或“不变”).
(4)接近饱和的丙溶液,在保持溶质质量分数不变的情况下转变为饱和溶液,可采取的方法是 .
(5)将t3℃时等质量的甲、乙两物质的饱和溶液,同时降温到t1℃,析出甲的质量 乙 (选填“>”“<”或“=”).
