制备高纯硅和二氧化硅主要工艺流程如图所示。
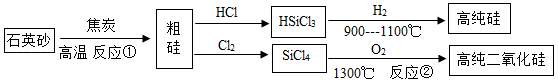
(1)2019年,我国华为公司推出了5G商用芯片。制造芯片要用到高纯硅,硅属于 元素(填"金属"或"非金属")。
(2)反应①的化学方程式为:SiO 2+2C  Si+2CO↑,从氧化还原反应角度分析,C发生了 反应。
Si+2CO↑,从氧化还原反应角度分析,C发生了 反应。
(3)用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为 。整个工艺流程中,还可以循环利用的另一种物质是 。
制备高纯硅和二氧化硅主要工艺流程如图所示。

(1)2019年,我国华为公司推出了5G商用芯片。制造芯片要用到高纯硅,硅属于 元素(填"金属"或"非金属")。
(2)反应①的化学方程式为:SiO 2+2C  Si+2CO↑,从氧化还原反应角度分析,C发生了 反应。
Si+2CO↑,从氧化还原反应角度分析,C发生了 反应。
(3)用于制造光导纤维的高纯二氧化硅,可利用反应②制备,同时生成一种可循环使用的物质,该反应的化学方程式为 。整个工艺流程中,还可以循环利用的另一种物质是 。